CORONAVIRUS
Pacientes vulnerables ya están recibiendo el antiviral de AstraZeneca frente al coronavirus
El fármaco, de nombre comercial Evusheld, forma parte del arsenal terapéutico para combatir el coronavirus y está indicado para personas inmunodeprimidas o con alergias severas a las vacunas.
España ha comprado 30.000 unidades de un fármaco que es de uso hospitalario y se administra como medida para prevenir la infección y el riesgo de desarrollar complicaciones en personas cuyo sistema inmunitario no funciona adecuadamente.
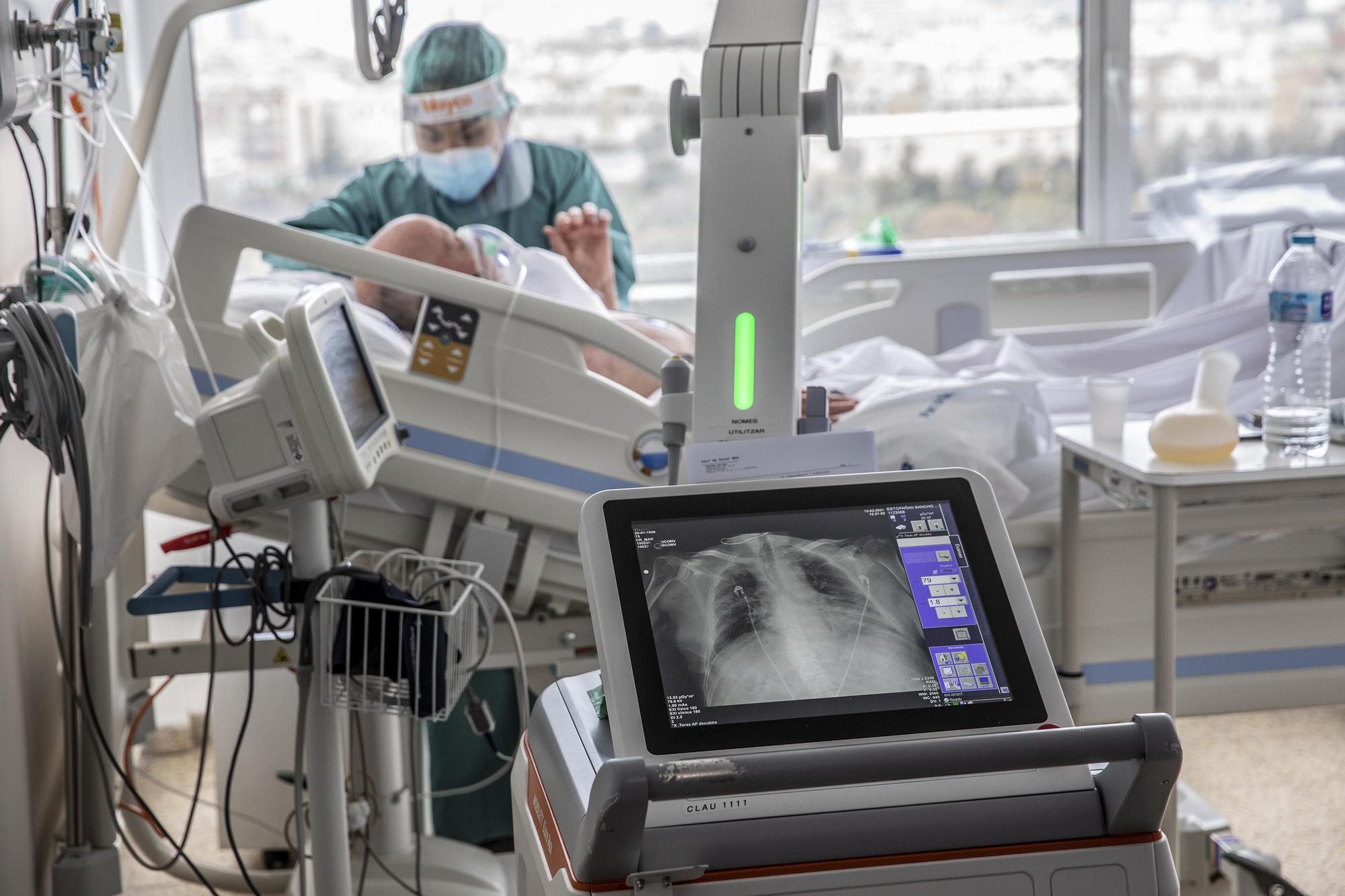
Planta covid hospital del Mar / Ferran Nadeu
El antiviral de AstraZeneca para la prevención del covid-19 en personas inmunodeprimidas o con alergias severas a las
vacunas
, ya está administrándose a pacientes españoles, según confirman fuentes del Ministerio de Sanidad a EL PERIÓDICO DE ESPAÑA. El fármaco, de nombre comercial Evusheld, forma parte del arsenal terapéutico para combatir el coronavirus del que dispondrá España en los próximos meses. Falta por llegar el medicamento oral de Pfizer para el tratamiento del covid-19 leve a moderado. El pasado enero, el Gobierno anunció que ese mes compraría 344.000 unidades del fármaco pero el tratamiento todavía no está en España.
El antiviral de AstraZeneca es, actualmente, el único medicamento que persigue una indicación de profilaxis pre exposición, es decir, como medida para prevenir la infección y el riesgo de desarrollar complicaciones en personas cuyo sistema inmunitario no funciona adecuadamente (inmunocomprometidas) desde trasplantadas de órganos sólidos o personas tratadas por neoplasias hematológicas con medicamentos que inhiben su capacidad de generar inmunidad frente al antígeno inyectado con las vacunas.
El fármaco, que es de uso hospitalario, ya se está administrando a pacientes españoles, según confirman fuentes de Sanidad a este diario. La ministra Carolina Darias y el presidente de AstraZeneca España, Rick Suárez, formalizaban a principios de febrero un acuerdo para el suministro y distribución del medicamento. A lo largo de ese mismo mes, nuestro país preveía cerrar la compra de 30.000 antivirales contra el coronavirus de la farmacéutica británica.
Seis perfiles de pacientes
El medicamento es una combinación de dos anticuerpos monoclonales (tixagevimab y cilgavimab), indicado para la inmunización pasiva de pacientes con más alto riesgo de contraer el covid-19 y de evolucionar a formas graves de la enfermedad. Se trata de un fármaco que, según la farmacéutica, podría beneficiar a un 2% de pacientes a nivel global. La Comisión de Salud Pública ha sido la encargada de establecer el perfil de los candidatos que recibirán el fármaco.

Carolina Darias y presidente de AstraZeneca España, Rick Suárez, en la firma del acuerdo. / Ministerio de Sanidad
Es la primera terapia con anticuerpos autorizada en
Estados Unidos
para la profilaxis previa a la exposición dirigida a poblaciones vulnerables. La terapia se encuentra aún en fase de revisión continua por parte de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés). Es decir, los países miembros pueden recurrir a él a través de los procesos habilitados para el uso de medicamentos, todavía no autorizados por dicho organismo.
De hecho, este mismo mes de marzo, la Agencia Europea de Medicamentos ha empezado a evaluar la solicitud de autorización de comercialización para el medicamento, tras la revisión continua que arrancó el pasado mes de octubre. La compañía emitió la petición y ha sido aceptada por el estamento comunitario. El fármaco, según el organismo, ha demostrado ser eficaz con la nueva subvariante surgida de una mutación de ómicron, la BA2.
¿Qué pasa con el antiviral de Pfizer?
Por otro lado, en cuanto Paxlovid, el medicamento oral de Pfizer que reduce en casi un 90% la posibilidad de hospitalización de los pacientes vulnerables, desde el Ministerio de Sanidad insisten en las últimas semanas en que se están dando todos los pasos para que esté aquí lo antes posible, aunque comunidades como Madrid ya han pedido al Gobierno que se acelere su llegada porque, en otros países, como Francia e Italia, ya está disponible.
El presidente Pedro Sánchez anunciaba en enero que, ese mismo mes, España compraría 344.000 dosis del medicamento para el tratamiento del covid-19 leve a moderado en pacientes adultos y adolescentes (a partir de 12 años de edad y con un peso mínimo de 40 kg) que no requieren oxígeno suplementario y presentan un alto riesgo de progresión a enfermedad grave. Sin embargo, el fármaco todavía no está disponible para los pacientes españoles.
Mutaciones y resistencias del virus
Este mismo lunes se ha conocido un estudio, de la Universidad de Rutgers, en Nueva Jersey, Estados Unidos, que confirma la eficacia del fármaco de Pfizer, pero advierte de las posibles mutaciones y resistencia del virus. La investigación, publicada en la revista Cell Research, es una de las primeras en explorar el alcance total de las mutaciones del SARS-CoV-2. Según este estudio, el fármaco Paxlovid es capaz de anular el covid-19 al bloquear la maquinaria celular de una proteína clave, conocida como la proteasa principal o Mpro, involucrada en la replicación del virus.
El covid-19 está comenzando a evolucionar de manera que puede producir cepas que pueden evadir los tratamientos actuales, según advierte un estudio.
Una de las principales conclusiones que han obtenido los investigadores, y por las que han dado la voz de alarma, es que han descubierto, a través del análisis genético, que el virus está comenzando a evolucionar de manera que puede producir cepas que pueden evadir los tratamientos actuales. Los científicos han explicado que la variante ómicron todavía es lo suficientemente nueva como para que los tratamientos sigan funcionando, pero han advertido que, a medida que más personas tomen el fármacos, la resistencia al medicamento puede ser mayor.
- Acciona se perfila como favorita para adjudicarse el 'megacontrato' de la reforma de la Estación de Sants
- RoRo, una máquina de vender publicidad con apariencia de 'tradwife' y una gran agencia detrás
- Xuan Lan, maestra del bienestar: 'La felicidad no es perder tres kilos e irse de vacaciones, es un viaje de autoconocimiento
- Fuenlabrada ultima los trámites para impedir la construcción de un centro para menores inmigrantes en La Cantueña
- Peinado estudia admitir a la Complutense como acusación en el caso Begoña Gómez aunque ha imputado a su rector
- El empresario recomendado por Begoña Gómez contesta a Peinado que 'carece de cualquier justificación citarle como investigado
- Lluís Homar cobró 5.000 euros por una adaptación de ‘La discreta enamorada’ que replicaba el trabajo de una investigadora valenciana
- Última hora del caso Daniel Sancho, en directo: todo lo que sabemos de Xenia Tostado, principal apoyo de Rodolfo Sancho durante el juicio de su hijo
